Cơ quan Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) đã công bố mức phí sử dụng thiết bị y tế mới cho năm tài chính 2025, có hiệu lực từ ngày 1 tháng 10 năm 2024, đồng thời nêu bật những cập nhật quan trọng nhằm tăng cường giám sát theo quy định và đảm bảo tính an toàn và hiệu quả của các thiết bị y tế.
Chương trình phí sử dụng của FDA được thiết kế để tạo ra các nguồn lực cần thiết cho các hoạt động quản lý của cơ quan, bao gồm đánh giá trước khi đưa ra thị trường, kiểm tra tuân thủ và giám sát sau khi đưa ra thị trường. Đối với năm tài chính 2025, lễ hội phí thiết bị mới của FDA bao gồm các khoản phí đã điều chỉnh trên một số danh mục, bao gồm:
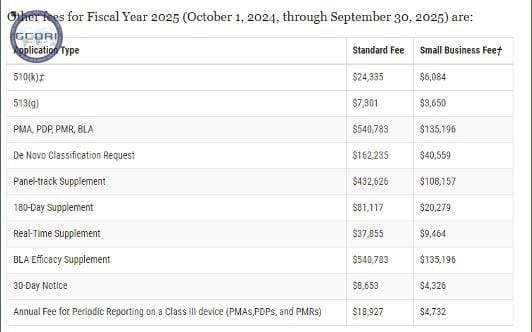
- Phí nộp đơn trước khi ra thị trường
- Phí đăng ký thành lập
- Phí niêm yết thiết bị
Những thay đổi chính trong Phí đăng ký thiết bị:
Chi phí tăng lên
Đối với năm tài chính 2025, FDA đã đề xuất tăng đáng kể phí đăng ký thiết bị, từ 7.653 đô la (năm tài chính 2024) lên 9.280 đô la (năm tài chính 2025). Việc điều chỉnh này nhằm mục đích phù hợp hơn với chi phí thực tế mà cơ quan này phải chịu trong việc quản lý quy trình đăng ký và đảm bảo tuân thủ các tiêu chuẩn quản lý. Các khoản phí tăng này dự kiến sẽ hỗ trợ các hoạt động quản lý nâng cao và giúp FDA tăng hiệu quả của quy trình đánh giá.
Cấu trúc phí theo từng bậc
Để giải quyết bối cảnh đa dạng của ngành thiết bị y tế, FDA tiếp tục triển khai cơ cấu phí theo từng bậc. Hệ thống này phân loại phí dựa trên quy mô doanh nghiệp:
Doanh nghiệp nhỏ : Các doanh nghiệp nhỏ đủ điều kiện sẽ tiếp tục được hưởng lợi từ việc giảm phí đăng ký, giảm bớt gánh nặng tài chính và khuyến khích đổi mới và thâm nhập thị trường cho những doanh nghiệp mới.
Các tập đoàn lớn : Các thực thể lớn hơn tiếp tục phải chịu mức phí cao hơn, phản ánh khả năng hấp thụ những chi phí này lớn hơn của họ.
Yêu cầu đăng ký hàng năm
Xin nhắc lại, tất cả các công ty sản xuất thiết bị phải tuân thủ các yêu cầu đăng ký thiết bị (nhà sản xuất, nhà phát triển thông số kỹ thuật, nhà xuất khẩu nước ngoài, nhà nhập khẩu thiết bị ban đầu, v.v.) đều phải gia hạn đăng ký thiết bị cho năm tài chính tiếp theo, bắt đầu từ ngày 1 tháng 10. Yêu cầu này nhằm mục đích duy trì sổ đăng ký thiết bị y tế chính xác và cập nhật, tạo điều kiện theo dõi hiệu quả hơn và phản hồi nhanh hơn trong trường hợp thu hồi hoặc các vấn đề về an toàn.
Vì một số lượng lớn các lệnh tạm giữ và từ chối nhập khẩu của FDA đối với các thiết bị y tế tập trung vào các cơ sở không có đăng ký thiết bị y tế và danh sách thiết bị theo yêu cầu, chúng tôi xin nhắc nhở các doanh nghiệp bị ảnh hưởng rằng việc không đăng ký cơ sở thiết bị y tế là hành vi bị cấm và có thể dẫn đến các hành động thực thi, bao gồm lệnh cấm hoặc truy tố. Các quy định của FDA quy định rằng việc một cơ sở thiết bị không đăng ký với FDA sẽ khiến các thiết bị được sản xuất hoặc chế biến tại cơ sở đó bị dán nhãn sai và do đó có thể bị từ chối nhập cảnh.
Chúng tôi nhắc nhở các doanh nghiệp tiếp tục sử dụng danh nghĩa phí và tuân thủ trước! Chúng tôi khuyên bạn nên hiểu và kết hợp các thay đổi về phí mới cho mục đích lập kế hoạch và đảm bảo tuân thủ kịp thời để giảm thiểu các vấn đề thực thi của FDA.
Để biết thêm thông tin về phí sử dụng thiết bị y tế mới của FDA, đăng ký và niêm yết thiết bị của FDA hoặc các câu hỏi chung về việc tuân thủ thiết bị y tế, vui lòng liên hệ với chúng tôi theo địa chỉ info@gcdri.com hoặc Hotline: 0904.889.859 (Ms.Hoa) – 0908.060.060 (Mr. Tiệp)
Xem thêm chi tiết về dịch vụ chứng nhận FDA tại đây: https://gcdri.com/dang-ky-chung-nhan-fda


